
发表期刊:Cell Reports
影响因子:9.995
发表时间:2022年10月25日
研究方法:m6A MeRIP-seq、MeRIP-qPCR、RIP-qPCR、RNA pull down
文章链接:m6A modification confers thermal vulnerability to HPV E7 oncotranscripts via reverse regulation of its reader protein IGF2BP1 upon heat stress
云序生物提供的服务

技术路线
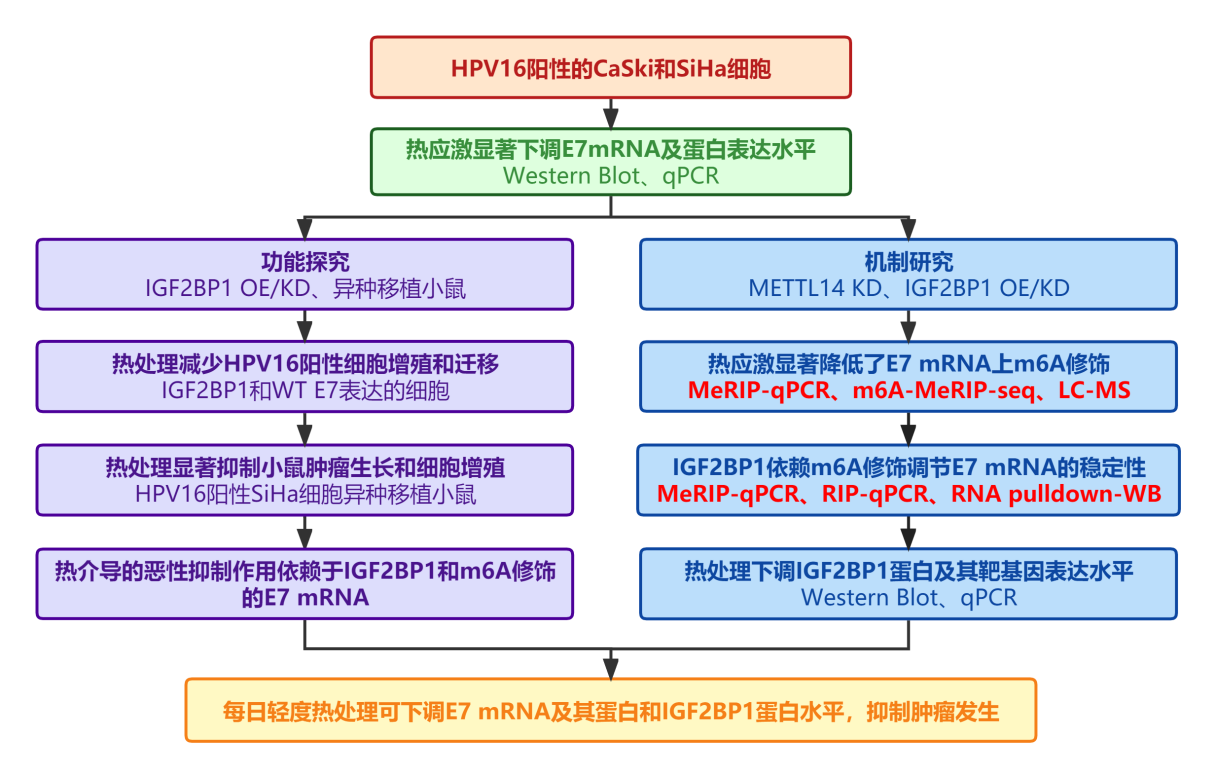
1. 热应激下调HPV16 E7 mRNA稳定性
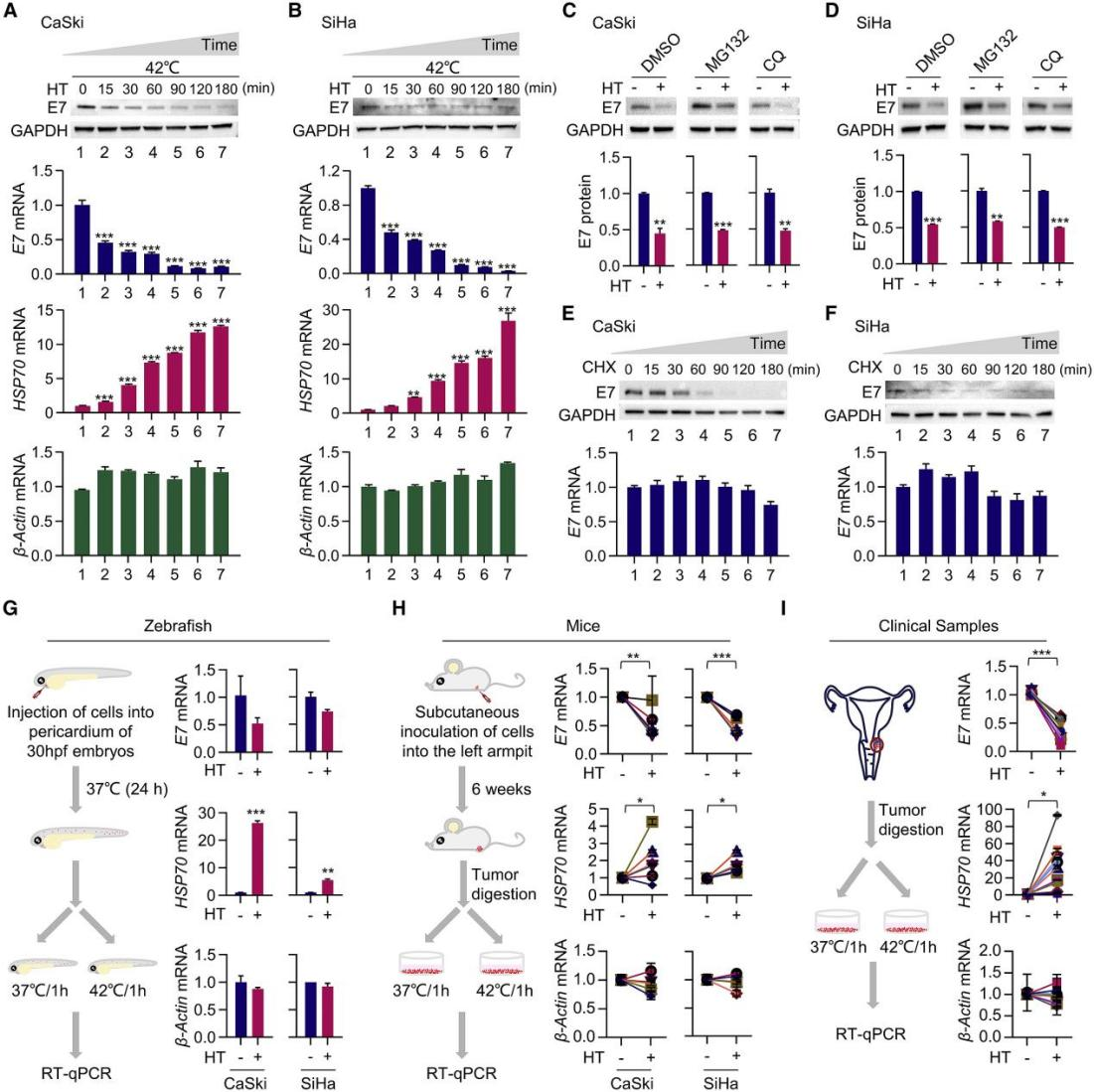
为了初步评估E7的热敏性,作者使用了HPV16阳性的CaSki和SiHa细胞,发现热应激以时间和温度依赖性的方式显著下调了E7蛋白及其mRNA的水平(图1A-B)。无论是蛋白酶体抑制剂MG132,还是溶酶体抑制剂氯喹(CQ)均不能挽救热处理导致的E7蛋白的下调(图1C-D),这表明热应激介导的E7 mRNA的下调是E7癌蛋白水平降低的主要原因。此外,作者发现在CaSki或SiHa移植的斑马鱼(图1G)和裸鼠(图1H)中,热处理后E7 mRNA水平下调。热处理也显著降低了hpv16阳性患者肿瘤样本中的E7 mRNA水平(图1I),这表明通过热处理来降低HPV16阳性肿瘤中的E7具有临床潜力。
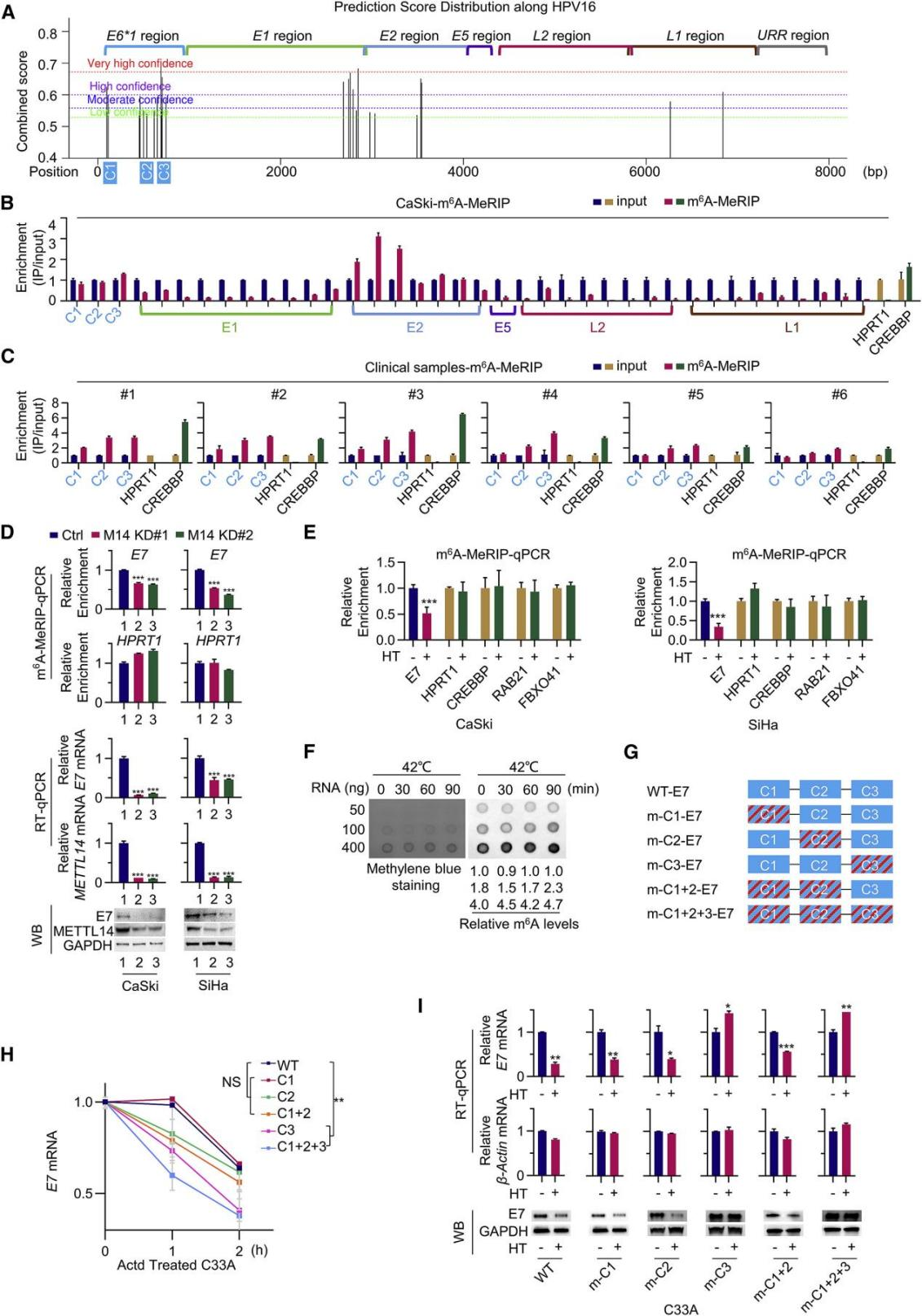
2. 热应激以m6A依赖的方式下调HPV16 E7 mRNA稳定性
由于m6A修饰是RNA代谢的关键调控因子,作者研究了m6A修饰是否参与了热诱导的E7 mRNA的下调。首先,作者使用SRAMP预测了产生E7癌蛋白的主要转录本HPV16 E6*1上三个潜在的m6A位点簇(C1、C1和C3)(图2A)。MeRIP-qPCR结果证实了在CaSki(图2B)和SiHa细胞(图2C)以及6例HPV16阳性患者的肿瘤样本中存在这些m6A位点簇。由于m6A修饰主要是由METTL3/METTL14复合物催化,作者用siRNAs敲除METTL14,发现E7转录本上的m6A水平显著降低,同时E7 mRNA及其蛋白表达水平下调(图2D)。这些结果表明,m6A对E7 mRNA的稳定性至关重要。重要的是,MeRIP-qPCR结果显示热应激显著降低了E7 mRNA上m6A修饰,而LC-MS/MS整体甲基化水平检测发现整体m6A水平无显著变化(图2E-F)。同样,m6A MeRIP-seq结果显示其他mRNA,包括CREBBP、RAB21和FBXO41的m6A水平不受温度升高的影响,进一步表明热应激选择性地降低E7 mRNA稳定性。接下来,作者为了进一步确定负责热敏感性的关键m6A位点,构建了一系列E7 mRNA的m6A位点特异性突变转录本(图2G)。结果发现,含有m6A位点簇C3突变的m7 mRNA的稳定性远低于完整C3区,且热处理只下调了具有完整C3区域的E7转录本及其蛋白产物(图2H-I)。综上所述,C3区m6A的修饰对E7 mRNA的稳定至关重要,并在热应激介导的E7 mRNA及其蛋白产物的下调中发挥了关键作用。
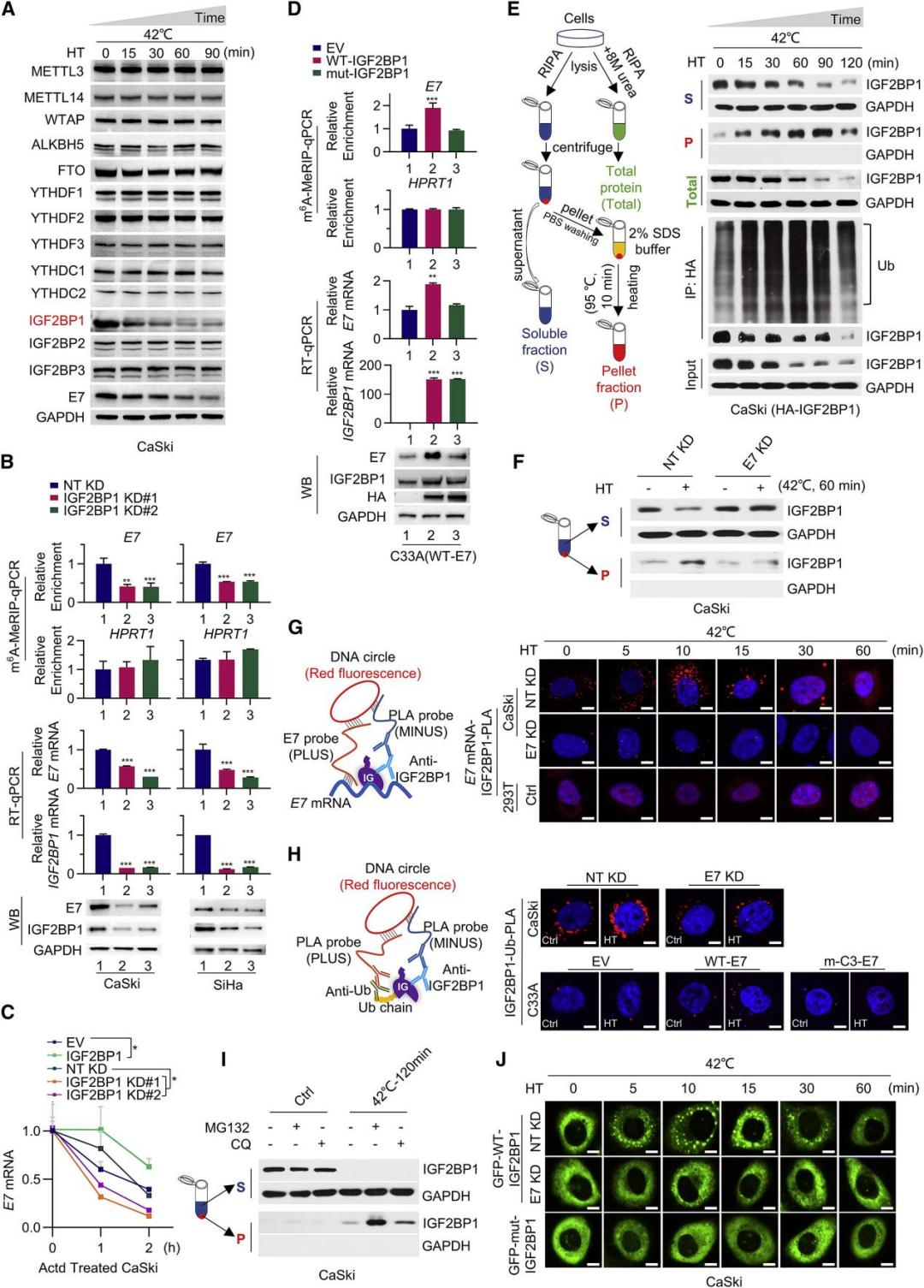
3. 热处理特异性下调E7 mRNA-IGF2BP1致癌复合物稳定性
接下来,作者研究了热处理通过m6A下调E7 mRNA的机制。通过评估高温对主要的m6A修饰酶的影响,作者发现只有m6A reader蛋白IGF2BP1在热应激下显著降低(图3A)。MeRIP-qPCR结果显示沉默IGF2BP1显著降低了E7 mRNA上的m6A水平,同时E7 mRNA和蛋白水平显著降低(图3B)。IGF2BP1的过表达稳定E7 mRNA,而IGF2BP1的缺失使E7 mRNA不稳定(图3C)。此外,RIP-qPCR以及RNA pulldown-WB的结果显示WT-IGF2BP1,而不是m6A结合缺陷的突变体mut-IGF2BP1结合、稳定并增加了E7 mRNA和蛋白的水平,支持了IGF2BP1以m6A依赖的方式调节E7 mRNA的稳定性的观点。在热处理后,IGF2BP1迅速从可溶性提取物转变为不可溶性颗粒组分随之泛素化,且E7的消耗在很大程度上抑制了热应激下可溶性IGF2BP1的减少(图3E),这表明IGF2BP1的不稳定可能是由于热诱导的E7依赖的IGF2BP1聚集造成的(图3E-F)。RIP-qPCR结果显示热处理后,E7 mRNA与IGF2BP1的相互作用迅速增强,然后逐渐减少。PLA检测显示IGF2BP1的热刺激泛素化只发生在WT E7表达细胞中,而不是在E7缺失或m6A突变体(m-C3)E7表达细胞中(图3H),支持了热介导的IGF2BP1泛素化是通过m6A修饰的E7 mRNA依赖的方式诱导的观点。与RNA-PLA的结果一致,GFP IGF2BP1在热处理后迅速形成了显微镜下可见的颗粒(图3J)。
4. 每日热处理可下调E7和IGF2BP1,并降低HPV阳性细胞的致瘤潜能
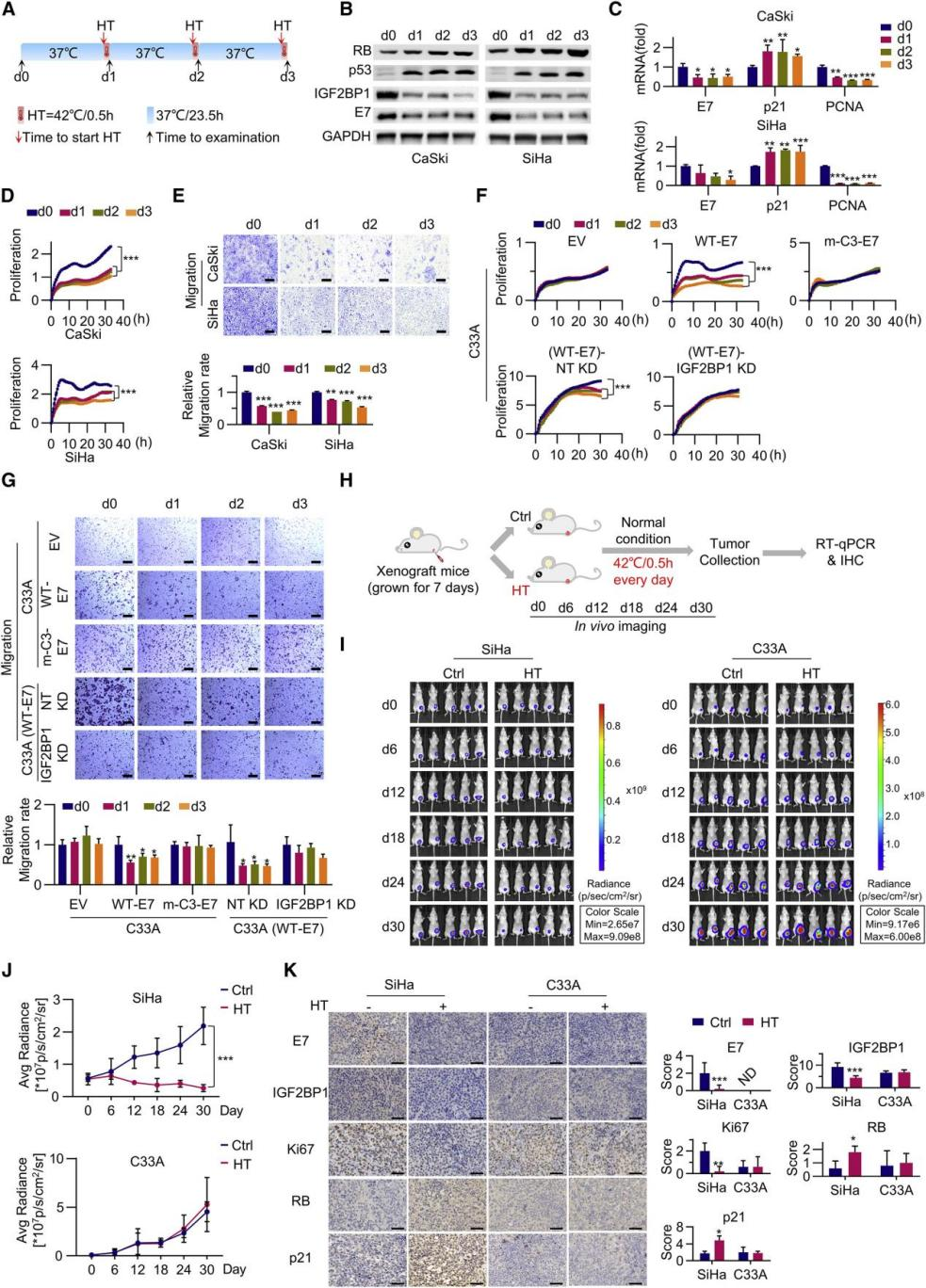
接下来,作者探讨了热应激介导的作用是否能抑制HPV16阳性细胞的恶性肿瘤。研究表明,每日短期(30 min)轻度热处理足以下调E7 mRNA及其E7蛋白产物和IGF2BP1蛋白水平,抑制RB和p53蛋白表达,导致p21(p53靶基因)表达上调,PCNA(E2F靶基因)表达下调,减少HPV16阳性细胞增殖和迁移(图4A-E)。值得注意的是,仅在IGF2BP1和WT E7表达的细胞中观察到热诱导p21上调、PCNA下调、细胞增殖和迁移减少,而在E7阴性、m6A突变(m-C3)E7和IGF2BP1敲降(IGF2BP1 KD)C33A细胞中未发现(图4F-G),表明这些热介导的恶性抑制作用依赖于IGF2BP1和m6A修饰的E7 mRNA。接下来,作者建立了异种移植小鼠模型,并检测了每日热处理30天的效果(图4H)。结果显示,每日热处理SiHa而不是C33A异种移植小鼠,显著抑制肿瘤生长和细胞增殖,下调E7 mRNA、E7蛋白和IGF2BP1蛋白,以及上调RB和p21蛋白(图4H-K)。综上所述,每日轻度热处理可下调E7,抑制肿瘤发生,提示其具有临床潜力。
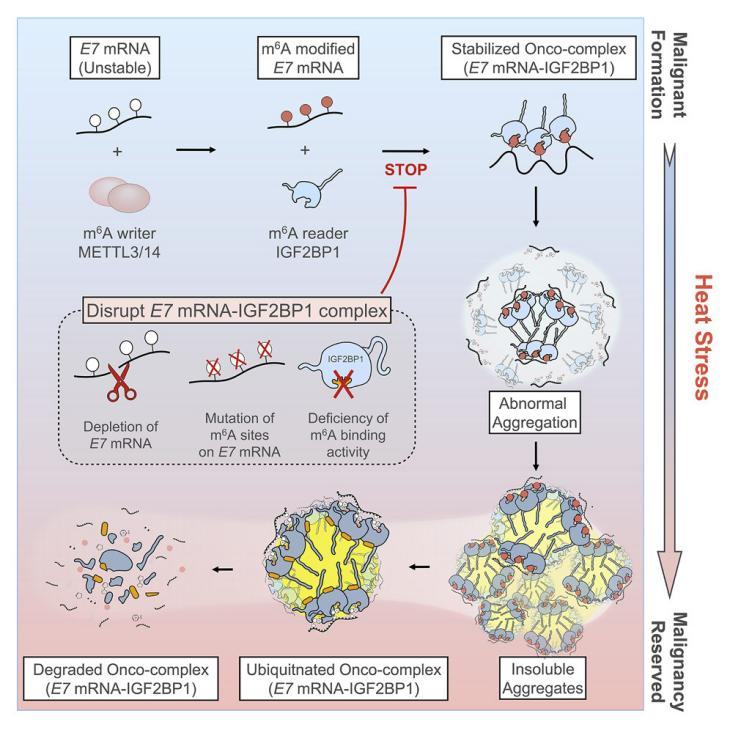
作者通过m6A MeRIP-seq、MeRIP-qPCR、RIP-qPCR、RNA pulldown等一系列实验发现在感染HPV的细胞中,病毒E7 mRNA被N6-甲基腺苷(m6A)修饰,并被reader蛋白IGF2BP1稳定。此外,本文研究发现,热处理选择性地破坏m6A修饰的HPV E7 mRNA,反向调节IGF2BP1,从而抑制E7介导的HPV阳性细胞的恶性肿瘤。
01 m6A RNA修饰测序
m6A RNA修饰测序(m6A-meRIP-seq)
对m6A RNA甲基化,目前最流行的检测手段为m6A-MeRIP-Seq技术,适用于m6A RNA甲基化谱研究,快速筛选m6A RNA甲基化靶基因。云序可提供mRNA和多种非编码RNA的m6A测序:
- m6A 全转录组测序(涵盖mRNA,LncRNA,circRNA)
- m6A LncRNA测序(涵盖LncRNA和mRNA)
- m6A Pri-miRNA测序(涵盖Pri-miRNA和mRNA)
- m6A mRNA测序
- m6A miRNA测序
LC-MS/MS检测整体RNA修饰水平
精准高效,可以实现一次检测,9类修饰水平检测,一步到位。
比色法检测整体RNA修饰水平
快速检测m6A整体甲基化水平
03 m6A RNA修饰上游酶的筛选
m6A RNA修饰相关酶PCR芯片
寻找上游直接调控m6A RNA甲基化的甲基转移酶。
04 m6A RNA修饰靶基因验证
MeRIP-qPCR/GenSeq® MeRIP试剂盒
云序提供各类不同修饰的meRIP-qPCR服务以及销售GenSeq® MeRIP试剂盒,可针对mRNA,lncRNA,环状RNA等不同类型的RNA分子进行检测,低通量验证RNA修饰靶基因表达水平。05 机制互作研究
5.1 RIP-seq/qPCR/GenSeq® RIP试剂盒筛选或验证RNA修饰直接靶点,研究RNA修饰靶基因的调控机制。
5.2 RNA pull down -MS/WB
筛选或验证目标RNA互作基因或蛋白,研究相应的分子调控机制。
5.3 双荧光素酶实验
验证两基因互作,研究相应的分子调控机制。
5.4 ChIP-seq
筛选或验证目标蛋白与DNA互作,研究相应的分子调控机制。
优势一:云序累计支持客户发表 84 +篇RNA修饰SCI论文,合计影响因子 814 +
优势二:累计完成数千例 RNA甲基化测序样本,全面覆盖医口、农口等各类样本。
优势三:全面检测mRNA和各类非编码RNA(circRNA,lncRNA,Pri-miRNA等)。
优势四:提供m6A一站式服务:m6A整体水平检测、m6A测序、MeRIP-qPCR验证、RIP和RNA pull-down等。
优势五:率先研发超微量MeRIP测序技术,RNA量低至500ng起。
优势六:国内较全的RNA修饰测序平台,提供m6A、m5C、m1A、m7G、m3C、O8G、ac4C乙酰化和2'-O-甲基化测序。
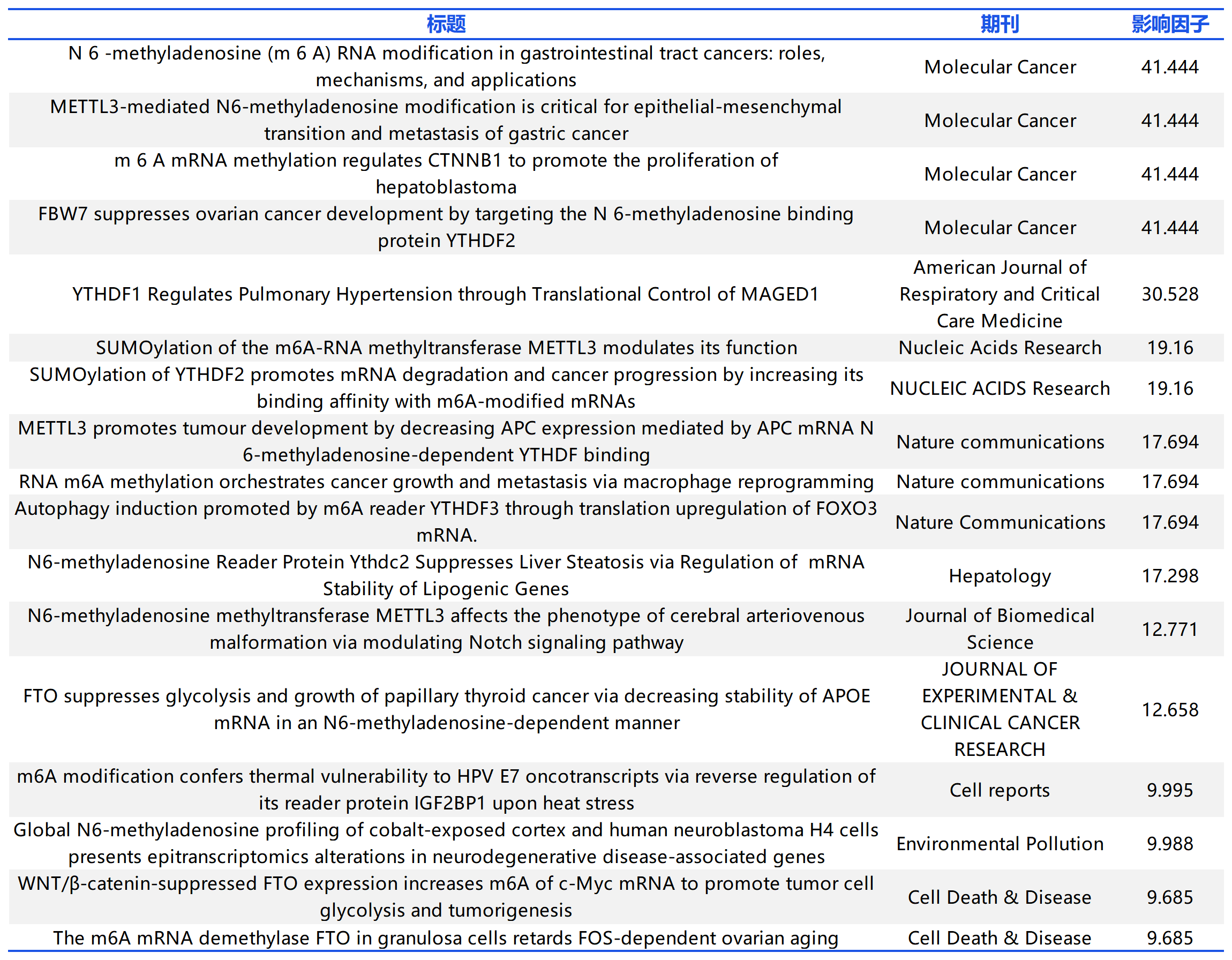
云序客户m6A高分文章列表
相关产品
上海云序生物科技有限公司 商家主页
地 址: 上海市松江区莘砖公路518号24号楼4楼
联系人: 戴小姐
电 话: 021-64878766
传 真: 021-64878766
Email:market@cloud-seq.com.cn;liuqingqing@cloud-seq.com.cn
相关咨询
杨宝峰院士团队RNA修饰又一成果 | 云序ac4C acRIP-seq助力揭示心脏I/R损伤的作用机制 (2024-12-03T00:00 浏览数:2548)
杨宝峰院士团队最新成果 | 云序助力揭示RNA修饰m7G调控心肌肥厚的机制研究 (2024-11-13T00:00 浏览数:4418)
Nature子刊| 重磅综述!一文总结「m6A修饰非编码RNAs」在各类肿瘤中的调控机制及作用 (暂无发布时间 浏览数:4153)
研究速览-eccDNA 2023年最新进展大放送! (暂无发布时间 浏览数:3812)
云序生物MeRIP-qPCR技术干货 (暂无发布时间 浏览数:3812)
技术干货| “eccDNA碱基序列的获取及引物设计”方法教程 (暂无发布时间 浏览数:4136)
云序客户m6A高分文章|揭示组蛋白乙酰化与m6A修饰在眼部黑色素瘤发生中的共同作用机制 (暂无发布时间 浏览数:2880)
Nat Biotechnol IF=47 | BID-seq:一种基于单碱基分辨率的假尿嘧啶(Ψ)修饰定量测序检测方法 (暂无发布时间 浏览数:2628)
北大伊成器团队Nature Reviews重磅发文:非m6A热门修饰调控与功能一文速览! (暂无发布时间 浏览数:3695)
用户文章m6A专题|IF=9.8|m6A去甲基化酶ALKBH5缺乏会加重钴致神经退行性损伤 (暂无发布时间 浏览数:2528)
